En el mundo de la medicina moderna, uno de los mayores desafíos es lograr que los medicamentos avanzados, especialmente las terapias génicas y proteicas, lleguen de manera efectiva y segura a las células objetivo dentro del cuerpo humano. La barrera celular y los procesos de degradación intracellular limitan severamente el rendimiento de muchos tratamientos innovadores. Sin embargo, recientes avances en la ingeniería de vesículas extracelulares (VE) prometen superar estos obstáculos y transformar radicalmente la manera en que se administran las terapias avanzadas. Las vesículas extracelulares son pequeñas burbujas o partículas liberadas por las células, que actúan como mensajeros naturales transportando moléculas biológicas entre células. Estas nanoestructuras biológicas juegan un papel esencial en la comunicación celular, llevando proteínas, ácidos nucleicos, lípidos y otras sustancias que influyen en funciones biológicas diversas.
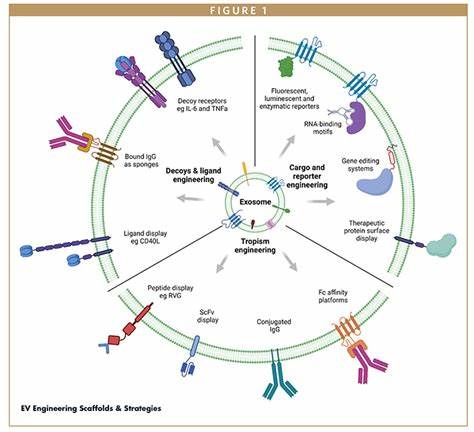
Aprovechar este mecanismo natural para la entrega de medicamentos ha sido un sueño para los investigadores durante años. Un equipo de científicos del Karolinska Institutet ha logrado avances significativos al desarrollar un sistema de vesículas extracelulares ingenierizadas con componentes específicos para mejorar la entrega intracelular de terapias avanzadas. Esta innovación, recientemente publicada en la prestigiosa revista Nature Communications, describe dos componentes clave introducidos en las VE: una pequeña porción de una proteína bacteriana llamada inteína y una proteína fusogénica derivada de virus. La proteína fusogénica juega un papel crucial facilitando la fusión de las vesículas con la membrana endosomal dentro de la célula receptora, permitiendo que el contenido terapéutico escape de los endosomas y entre al citoplasma celular. Esta etapa es fundamental para evitar que los medicamentos sean degradados en el interior celular antes de alcanzar su objetivo.
Por su parte, la inteína tiene la capacidad de autoescindirse, ayudando a liberar de manera controlada las proteínas terapéuticas dentro de la célula, maximizando así su eficacia. Este sistema, denominado VEDIC y VFIC, demuestra una alta eficiencia para la entrega intracelular de proteínas terapéuticas y complejos de edición genética, como Cas9 y sgRNA, que forman parte de la tecnología CRISPR/Cas9. En estudios in vitro y en modelos animales, las vesículas diseñadas lograron no solo entregar estos biomoléculas sino también generar efectos biológicos significativos, como modificaciones genéticas en células del hipocampo y la corteza cerebral de ratones. Los resultados de los ensayos en animales son especialmente prometedores para el tratamiento de enfermedades neurodegenerativas y genéticas que afectan el sistema nervioso central, como la enfermedad de Huntington y la atrofia muscular espinal. La capacidad de llevar herramientas moleculares complejas directamente al cerebro, cruzando barreras biológicas difíciles, podría abrir la puerta a terapias personalizadas y efectivas para estos padecimientos hasta ahora incurables.
Adicionalmente, los investigadores observaron que la plataforma de vesículas extracelulares puede ser adaptada para combatir inflamaciones sistémicas, lo cual amplía aún más su potencial terapéutico. La versatilidad del sistema permite concebir aplicaciones para una variedad de condiciones médicas, desde enfermedades autoinmunes hasta trastornos metabólicos. Uno de los aspectos más destacables de esta tecnología es su naturaleza biocompatible y biodegradable, pues las vesículas extracelulares son producidas por células vivas y cargadas con moléculas terapéuticas mediante un proceso de ingeniería genética y bioquímica avanzado. Esto evita las respuestas inmunológicas adversas asociadas comúnmente con otros sistemas de entrega, como nanopartículas sintéticas o vectores virales modificados. A nivel molecular, la incorporación de la inteína como mecanismo autoescindible representa una innovación inteligente.
Las inteínas funcionan como tijeras moleculares que pueden activarse en respuesta a señales específicas dentro de la célula, liberando con precisión el componente terapéutico en el momento oportuno y en la localización correcta. Esto reduce la pérdida de fármaco y mejora la concentración en el sitio de acción. La proteína fusogénica, por otro lado, proviene de virus que han desarrollado a lo largo de la evolución mecanismos eficientes para fusionarse con membranas celulares e ingresar al interior de las células. Al incorporar esta proteína en las vesículas, los investigadores imitan estas estrategias naturales para maximizar la entrega y evitar barreras celulares que dificultan el ingreso de terapias macromoleculares. Este enfoque es capaz de sortear uno de los mayores retos de las terapias basadas en proteínas y genes: la evasión de la degradación lisosomal y endosomal, que suelen capturar y destruir los agentes terapéuticos antes de que cumplan su función.
La investigación impulsada por el Karolinska Institutet también destaca la importancia del diseño inteligente en la nanotecnología biomédica. La integración de diversos elementos biológicos y sintéticos dentro de una única plataforma optimiza la compatibilidad, eficacia y seguridad del tratamiento, reduciendo efectos secundarios y mejorando los perfiles farmacodinámicos. La eficiencia demostrada en múltiples sistemas celulares y tejidos animales sugiere que esta plataforma tiene un gran potencial de escalabilidad y adaptación para aplicaciones clínicas futuras. Esto incluye el desarrollo de terapias génicas dirigidas a distintos órganos, tratamientos personalizados para trastornos hereditarios raros y nuevas modalidades contra enfermedades inflamatorias crónicas. Además, la versatilidad del sistema abre las puertas a la entrega de otras moléculas terapéuticas complejas, como ARN mensajero, proteínas funcionales no codificantes y moduladores epigenéticos, ampliando el arsenal para combatir diversas patologías.
En términos de perspectiva clínica, las vesículas extracelulares diseñadas podrían transformar la manera en que se manejan enfermedades que hoy en día requieren tratamientos invasivos, costosos y con frecuentes efectos adversos. La posibilidad de administrar terapias potentes de forma más precisa, con menor toxicidad y mejor penetración tisular, revolucionará la farmacoterapia avanzada. Los desafíos técnicos pendientes incluyen la producción masiva y estandarizada de vesículas, la optimización de la carga terapéutica y la minimización de posibles reacciones inmunitarias imprevistas en humanos. Sin embargo, el trabajo pionero realizado ya marca un camino claro hacia la superación de estos obstáculos. Este avance científico también tiene implicaciones importantes para la medicina personalizada y la terapia regenerativa.
Al permitir la entrega eficiente de factores de crecimiento, moduladores genéticos o proteínas reparadoras directamente en células dañadas o enfermas, las vesículas extracelulares diseñadas podrían acelerar la recuperación de tejidos, influir en la plasticidad celular y promover la restauración funcional. La nanotecnología aplicada a la medicina, representada por esta innovadora plataforma de vesículas, simboliza la convergencia de múltiples disciplinas científicas: biología molecular, ingeniería genética, virología, farmacología y medicina clínica. Esta colaboración multidisciplinaria será crucial para traducir los hallazgos en terapias efectivas y accesibles. En conclusión, la ingeniería avanzada de vesículas extracelulares marca un antes y un después en la entrega de medicamentos y terapias avanzadas. Su capacidad para transportar de manera segura y eficaz proteínas terapéuticas y editores genéticos directamente a las células objetivo ofrece una solución prometedora a los retos de la medicina moderna.
Con continuos avances en esta área, el panorama terapéutico global está al borde de una completa transformación, con beneficios potenciales para millones de pacientes en todo el mundo.