El diagnóstico rápido y preciso de infecciones bacterianas es un desafío crítico en la medicina moderna. Tradicionalmente, la identificación de patógenos infecciosos depende de métodos que requieren el aislamiento y cultivo de bacterias, un proceso que puede tomar varios días antes de obtener resultados concluyentes. Esta demora puede complicar enormemente el tratamiento oportuno, afectando la recuperación del paciente y aumentando riesgos de complicaciones graves. No obstante, recientes avances científicos están marcando un antes y un después en esta área, gracias al desarrollo de una innovadora técnica que utiliza la espectrometría de masas para identificar bacterias directamente en muestras clínicas en cuestión de minutos, revolucionando los tiempos y la efectividad en el diagnóstico microbiológico. La espectrometría de masas es una tecnología analítica que permite identificar moléculas basándose en su masa y estructura química.
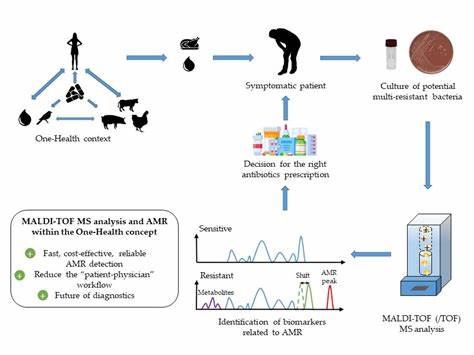
Su empleo ha sido tradicionalmente más común en química o bioquímica, pero científicos del Technical University Munich (TUM) y del Imperial College London han aplicado su potencial a la detección directa de patógenos. En lugar de buscar las bacterias enteras o sus secuencias genéticas, esta metodologia se centra en detectar los productos metabólicos que secretan las bacterias. Estos metabolitos actúan como biomarcadores específicos que permiten la identificación indirecta pero rápida del microorganismo causante de la infección. El núcleo de este método innovador es una base de datos que contiene información sobre 232 especies bacterianas médicamente relevantes y sus productos metabólicos asociados. Al detectar dichas moléculas características en muestras de tejido o heces mediante espectrometría de masas, el equipo científico puede identificar rápidamente la presencia de ciertos patógenos sin necesidad de cultivo.
Esto reduce el tiempo de diagnóstico de días a minutos, un avance trascendental que puede salvar vidas y optimizar el uso de antibióticos. Entre las bacterias identificables con esta técnica se encuentran algunas de gran impacto clínico, como aquellas que causan cáncer gástrico, neumonía, meningitis, parto prematuro, gonorrea y septicemia. La capacidad de detectar estos mismos microorganismos con rapidez permite que los médicos ajusten tratamientos específicos de manera temprana, mejorando significativamente las posibilidades de éxito y minimizando efectos secundarios derivados del uso innecesario o incorrecto de antibióticos. Wei Chen, estudiante de doctorado en el Departamento de Biosciencias de la TUM, señala que el concepto innovador radica en no buscar directamente el patógeno, sino en identificar sus productos metabólicos, lo cual acelera notablemente el proceso diagnosticador. Este enfoque indirecto, basado en metabolómica, supera limitaciones de métodos convencionales y puede ser integrado perfectamente con tecnologías existentes para diagnóstico clínico rápido y fiable.
La profesora Nicole Strittmatter, líder del grupo de química analítica en TUM, destaca las importantes implicaciones para la medicina personalizada. Al tener a disposición una herramienta que identifique con exactitud y rapidez los microorganismos causantes de infecciones, los tratamientos podrán ser diseñados específicamente según las necesidades individuales de cada paciente. Esta precisión reduce resistencias bacterianas, evita terapias empíricas y abre la puerta a intervenciones médicas mucho más efectivas y seguras. Aunque el progreso es notable, la expansión de la base de datos es una tarea clave hacia la implementación clínica masiva. Actualmente, existen identificados más de 1,400 patógenos bacterianos, muchos de los cuales carecen aún de sus perfiles metabólicos característicos registrados.
Ampliar esta base permitirá que la tecnología detecte un espectro más amplio de infecciones, consolidando la espectrometría de masas como un estándar en microbiología clínica. Esta técnica también muestra ventajas sobre otros métodos moleculares, como la hibridación in situ por fluorescencia (FISH), al proporcionar imágenes mas precisas mediante la espectrometría de masas (MSI) y permitir distinguir metabolitos específicos con alta sensibilidad y selectividad. La integración de ambas tecnologías puede potenciar todavía más las capacidades diagnósticas en laboratorios especializados. El impacto de esta innovación va más allá del ámbito hospitalario, pues puede influir en sectores como el control de calidad alimentaria y la producción farmacéutica, donde la detección rápida de contaminantes bacterianos es esencial para garantizar la seguridad. De igual forma, en la industria biotecnológica, el entendimiento detallado de metabolitos bacterianos abre nuevas vías para el desarrollo de fármacos y terapias dirigidas.


![Denmark says goodbye to letters [video]](/images/737CE4EB-9A5A-40FD-A92E-5C63C01E0CB1)