La salud mental representa uno de los desafíos más complejos y urgentes en la medicina contemporánea. Trastornos tan prevalentes como la depresión mayor, la ansiedad generalizada, el trastorno por estrés postraumático y otros trastornos relacionados con el trauma, impactan negativamente la calidad de vida de millones de personas a nivel mundial. La amígdala, un núcleo subcortical profundo del cerebro, ha sido identificado como una estructura clave en la regulación de las emociones, la detección de estímulos salientes y las respuestas adaptativas tanto fisiológicas como conductuales. Por ello, la neuromodulación dirigida de la amígdala surge como una vía prometedora para intervenir en estas patologías que a menudo resisten las opciones tradicionales de tratamiento. Durante décadas, el campo de la neuromodulación cerebral ha experimentado progresos considerables mediante técnicas como la estimulación magnética transcraneal (TMS) y la estimulación cerebral profunda (DBS).
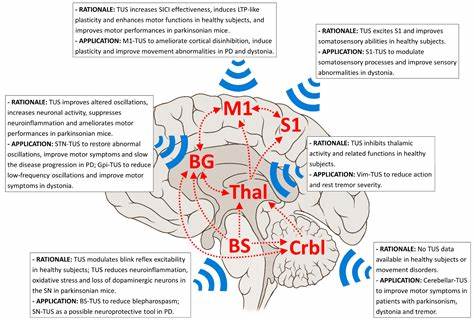
Sin embargo, la mayoría de las tecnologías no invasivas enfrentan la limitación de dirigirse principalmente a áreas corticales superficiales, teniendo que modular con indirecta la actividad de estructuras subcorticales profundas, como la amígdala, a través de redes neuronales. Esto reduce la precisión y eficacia potencial del tratamiento, además de depender de la integridad funcional de conexiones cortico-subcorticales que podrían encontrarse comprometidas en numerosas enfermedades psiquiátricas. El ultrasonido focalizado transcraneal de baja intensidad (tFUS) emerge como una innovadora herramienta capaz de superar estas barreras. Al utilizar ondas sonoras de alta frecuencia, este método no invasivo se focaliza con gran precisión en regiones cerebrales profundas, permitiendo la modulación directa de estructuras específicas como la amígdala. Sus mecanismos combinan efectos mecánicos que modulan canales iónicos sensibles al estímulo sonoro y potenciales efectos térmicos mínimos, ofreciendo una neuromodulación reversible sin daños tisulares evidentes.
Estudios recientes demuestran que la aplicación dirigida de tFUS a la amígdala izquierda puede suprimir su actividad funcional, medida mediante técnicas de imagen funcional por resonancia magnética (fMRI) que detectan cambios en el nivel de oxigenación sanguínea, indicador indirecto de actividad neuronal. En pacientes con trastornos del estado de ánimo, ansiedad y trauma, esta supresión se asocia con cambios en circuitos conectados, como el hipocampo y la ínsula, reflejando la capacidad del tFUS para alterar redes neuronales implicadas en la regulación emocional y la percepción del dolor o estrés. Asimismo, la modulación contralateral observada en estos estudios subraya la importancia de las conexiones interhemisféricas y abre preguntas acerca de cómo estas podrían mediar efectos terapéuticos más amplios. Un aspecto fundamental para cualquier nueva intervención es la seguridad y tolerabilidad, aspectos que el tFUS cumple satisfactoriamente. En múltiples reportes, incluyendo recientes ensayos clínicos piloto, no se han registrado eventos adversos graves, siendo los efectos secundarios leves y transitorios.
Estos pueden incluir sensaciones de hormigueo, cefalea o aumento momentáneo de irritabilidad en algunos casos, pero suelen resolverse sin intervención adicional. La alta tasa de finalización del tratamiento en protocolos diarios de tres semanas resalta la viabilidad en entornos clínicos y la buena aceptación por parte de los pacientes. Los resultados clínicos preliminares muestran reducciones significativas en síntomas de angustia general, depresión y ansiedad tras la administración repetida de tFUS a la amígdala. Aunque estos estudios carecen aún de controles rigurosos y son exploratorios, el tamaño del efecto observado es prometedor y comparable al de algunas intervenciones farmacológicas y psicoterapéuticas. La relación entre la disminución en la activación de la amígdala y la mejora clínica sugiere que la neuromodulación focalizada no solo altera la neurofisiología sino que también puede traducirse en beneficios reales para los síntomas del paciente.
Los paradigmas experimentales utilizados incluyen tareas de reconocimiento y emparejamiento de expresiones faciales emocionales, las cuales activan con fiabilidad la amígdala y permiten medir cambios funcionales específicos provocados por la neuromodulación. Notablemente, el procesamiento de rostros con expresiones de ira, conocidos por activar intensamente esta estructura, muestra una reducción posintervención más marcada. Estos hallazgos aportan evidencia mecanística y validan la especificidad del enfoque. A pesar de las ventajas, es importante reconocer las limitaciones actuales. El número reducido de participantes junto con la heterogeneidad diagnóstica implica la necesidad de estudios médicos controlados más amplios y bien diseñados para confirmar la eficacia y explorar diferencias según perfiles clínicos.
Además, el uso de medidas autoinformadas, aunque práctico y válido, debería complementarse con evaluaciones clínicas directas y biomarcadores objetivos en futuros trabajos. Por otra parte, la optimización técnica del tFUS continúa en desarrollo. El modelado acústico individualizado basado en la anatomía craneal podría mejorar la precisión y consistencia en la entrega de ultrasonidos, superando variables como el grosor y curvatura ósea que afectan la penetración del ultrasonido. La incorporación de estas tecnologías garantizará que la energía alcanzada en la amígdala sea adecuada y reproducible, incrementando el potencial terapéutico. El campo de la neuromodulación cerebral asistida por ultrasonidos focalizados avanza rápidamente y se posiciona como una posible revolución en el tratamiento de trastornos psiquiátricos resistentes o insuficientemente tratados.