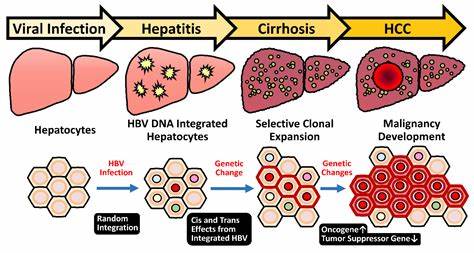
El papel del genoma del virus de la hepatitis B y su integración en el carcinoma hepatocelular El carcinoma hepatocelular (CHC) es uno de los tipos de cáncer más comunes y letales en el mundo. Se estima que las infecciones crónicas por el virus de la hepatitis B (VHB) son una de las principales causas de este tipo de cáncer. La relación entre el VHB y el CHC ha sido objeto de intensos estudios que han revelado los mecanismos complejos por los cuales este virus contribuye a la carcinogénesis hepática. En este contexto, surge una cuestión crucial: ¿cómo el genoma del VHB se integra en el ADN del huésped y qué efectos tiene esta integración en la función celular? El VHB pertenece a la familia Hepadnaviridae y su genoma está compuesto por ADN de doble cadena. Este virus tiene la capacidad de infectar las células hepáticas, donde se replica y puede provocar diversas alteraciones genéticas.
Uno de los fenómenos más relevantes asociados a la infección por VHB es la integración de su ADN en el genoma del hepatocito, que se ha demostrado que está estrechamente relacionada con el desarrollo de CHC. Los estudios recientes han identificado que la integración del genoma del VHB en el ADN humano normalmente ocurre en sitios específicos del genoma, conocidos como "sitios de integración preferenciales". Estos sitios no solo se encuentran en regiones genéticas que son sensibles a la ruptura, sino que también están asociados con genes que regulan procesos importantes como el crecimiento celular y la apoptosis. Cuando el VHB se integra en estos genes, puede alterar su función normal, llevando a una proliferación celular descontrolada y, a su vez, contribuyendo a la formación de tumores. Un aspecto fascinante de la integración del VHB es la posibilidad de que el ADN viral se convierta en formas extrachromosómicas al desprenderse de los cromosomas.
Estas formas de ADN, que existen independientemente del genoma del huésped, también pueden jugar un papel en la carcinogénesis. La presencia de ADN viral extrachromosómico puede ocasionar inestabilidad genómica, lo que incrementa el riesgo de que se produzcan mutaciones y alteraciones en el genoma del hepatocito. La regulación de la expresión de los genes tumorales en el contexto de la infección por VHB se lleva a cabo a través de la producción de proteínas virales, siendo la proteína X del VHB (HBx) uno de los actores clave en este proceso. La HBx se ha relacionado directamente con la activación de diversas vías de señalización celulares que promueven la proliferación celular y la supervivencia. Además, la HBx puede interferir con la actividad de proteínas supresoras de tumores, debilitando así las defensas naturales del cuerpo contra el cáncer.
A medida que se acumulan datos sobre los mecanismos de integración del VHB y su contribución al CHC, se vuelve evidente que la inestabilidadgenética resultante de estos eventos puede dar lugar a una serie de alteraciones celulares relevantes. La pérdida o ganancia de material genético, la formación de translocaciones e inversiones cromosómicas, así como la activación de oncogenes son estrategias que el virus utiliza para facilitar su persistencia y promover la transformación maligna de las células hepáticas. Un estudio reciente que investigó la integración del VHB en el genoma humano reveló que la presencia de secuencias de ADN del virus en diferentes regiones del genoma está relacionada con una mayor probabilidad de desarrollo de HCC. Este hallazgo sugiere que el análisis de los patrones de integración del VHB podría ofrecer información valiosa para la evaluación del riesgo de desarrollar cáncer en pacientes con hepatitis B crónica. Además, el uso de tecnologías avanzadas como la secuenciación de próxima generación está revolucionando nuestra comprensión de la integración del VHB, permitiendo identificar nuevas ubicaciones de integración y patrones que antes eran difíciles de discernir.
A medida que la investigación avanza, también se exploran las estrategias para abordar la infección por VHB desde una perspectiva terapéutica. El objetivo final es desarrollar tratamientos que no solo eliminen el virus del organismo, sino que también corrijan las alteraciones genéticas causadas por la integración del VHB. Las tecnologías emergentes, como la edición genética CRISPR/Cas9, ofrecen un enfoque potencialmente prometedor para eliminar el ADN viral integrado y reparar las lesiones genómicas que contribuyen a la carcinogénesis. En resumen, la integración del genoma del virus de la hepatitis B en el ADN del huésped juega un papel crítico en el desarrollo del carcinoma hepatocelular. La comprensión de estos mecanismos de integración y su impacto en la inestabilidad genómica y en la regulación de las vías de señalización celular abre nuevas posibilidades para el diagnóstico y tratamiento de esta enfermedad devastadora.
Se espera que con el avance de la investigación en virología y genética, se puedan desarrollar estrategias más efectivas para el manejo del CHC, así como para la prevención de la infección por VHB y su progresión a cáncer. Este campo de estudio no solo tiene implicaciones fundamentales para la biología del cáncer, sino que también podría revolucionar la forma en que abordamos la hepatitis viral en el futuro, mejorando así la calidad de vida de millones de personas en todo el mundo.