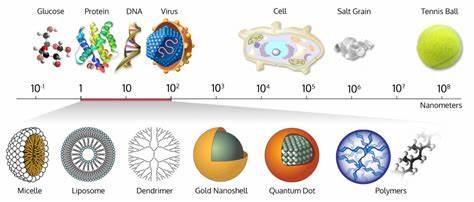
La medición del tamaño y la forma de las moléculas es fundamental para comprender numerosos procesos biológicos, químicos y físicos que rigen nuestro entorno. La estructura molecular determina cómo interactúan las biomoléculas, influye en su función y afecta la eficacia de fármacos, diagnósticos y materiales avanzados. Sin embargo, analizar estas propiedades de forma rápida, precisa y en condiciones nativas siempre ha sido un desafío para los científicos. Hoy en día, las tecnologías basadas en microchips emergen como una solución innovadora para abordar estas limitaciones, ofreciendo un método ultrarrápido y de alta sensibilidad para estudiar moléculas individuales en solución. Los avances en microfluídica y nanotecnología han llevado al desarrollo de plataformas miniaturizadas capaces de monitorear la movilidad y comportamiento molecular en espacios confinados.
Uno de los métodos más novedosos es la estereometría del tiempo de escape (ETs, por sus siglas en inglés), que permite evaluar simultáneamente el tamaño hidrodinámico y la forma tridimensional de especies moleculares, utilizando microchips con estructuras nanométricas diseñadas para fomentar atrapamientos entrópicos adaptados a la conformación molecular. Esta tecnología aprovecha el movimiento aleatorio de moléculas fluorescentes en canales especialmente diseñados con pequeñas trampas o indentaciones que ralentizan el desplazamiento de moléculas más grandes en comparación con las más pequeñas. La medida del tiempo que tarda una molécula en escapar de estas regiones restringidas está directamente relacionada con su tamaño efectivo y su conformación espacial. Este enfoque permite un análisis de alta resolución en tiempo real, que supera las tecnologías convencionales como la espectroscopía o la cristalografía, al ofrecer observación individualizada sin necesidad de procesos invasivos o marcadores complejos. Además, la precisión de ETs permite distinguir diferencias moleculares mínimas, como variaciones en solo dos átomos de carbono en pequeñas moléculas, algo impensable en métodos tradicionales.
Su sensibilidad apunta a detectar concentraciones extremadamente bajas, en rangos de femtomolar, lo que posibilita trabajar con muestras muy limitadas o escasas. Tal potencial representa un salto cualitativo para estudios de reacciones bioquímicas, cinéticas moleculares y detección de heterogeneidad en poblaciones moleculares, atendiendo a conformaciones alternativas o estados transitorios. Por otro lado, esta tecnología contribuye a la cuantificación detallada de interacciones intermoleculares, ofreciendo datos termodinámicos y cinéticos sobre afinidades y velocidades de disociación en una amplia escala dinámica. La capacidad para monitorear en tiempo real asociaciones y disociaciones moleculares en contexto líquido brinda un nivel de comprensión esencial para el diseño racional de fármacos, biosensores y sistemas de diagnóstico. La aplicación práctica de la medición del tamaño y la forma molecular en microchips es particularmente relevante en el ámbito biomédico.
Por ejemplo, el análisis de conformaciones del receptor de insulina ha demostrado ser una herramienta prometedora para la detección de niveles de insulina en suero, utilizando cambios conformacionales inducidos por ligandos como señal detectable en volúmenes subnanolitro y cantidades subzeptomolares, lo que supone una innovación para diagnósticos de diabetes y monitoreo clínico. Este método también soporta la investigación de complejos multiméricos formados a través de interacciones débiles, a menudo difíciles de identificar con técnicas convencionales. La posibilidad de obtener mapeos conformacionales a gran escala y con alta resolución prepara el terreno para integrar estos datos en sistemas de aprendizaje automático orientados a predecir y validar estructuras tridimensionales de proteínas, ARN y otras biomoléculas complicadas como aquellas inherentemente desordenadas. El enfoque basado en microchips, por su naturaleza paralela y escalable, ofrece además un alto rendimiento que favorece el procesamiento masivo de muestras. Esto lo convierte en una plataforma tecnológica atractiva para futuras aplicaciones industriales, farmacéuticas y de investigación básica, donde la rapidez combinada con una precisión sin precedentes es crítica para desarrollar soluciones personalizadas.
El desarrollo de la estereometría del tiempo de escape refleja un proceso interdisciplinario que ha reunido la física, la química, la biología molecular y la ingeniería de microfluídica, logrado gracias a la colaboración entre distintas universidades e institutos de investigación. Este progreso es un claro ejemplo de cómo la integración tecnológica puede superar los límites tradicionales de caracterización molecular, abriendo la puerta a un análisis más profundo y controlado de la diversidad biomolecular. Para comprender más a fondo el impacto que estas técnicas tienen, es fundamental considerar la importancia del tamaño molecular y la forma en su función biológica y química. Por ejemplo, las proteínas adoptan conformaciones específicas que definen su actividad enzimática o de señalización, mientras que los ácidos nucleicos necesitan plegarse en estructuras precisas para regular la expresión genética o participar en ensamblajes moleculares más complejos. La dinámica conformacional, incluida la existencia de estados intermedios o desordenados, puede ser decisiva en enfermedades neurodegenerativas, plegado erróneo, agregación proteica o resistencia farmacológica.