El cáncer representa uno de los mayores retos médicos y científicos de nuestro tiempo. A pesar de los avances logrados en la oncología, ciertos tipos de cáncer, especialmente los que afectan a la infancia, siguen siendo devastadores y difíciles de tratar con la medicina convencional. Sin embargo, una innovación emergente en el campo de la farmacología, conocida como PROTACs (siglas en inglés de proteolysis-targeting chimeras o quimeras de degradación dirigida de proteínas), está generando un gran optimismo. Estos medicamentos tienen el potencial de atacar y eliminar las proteínas causantes de enfermedades, incluyendo las que durante décadas han sido consideradas “indrugables” o imposibles de tratar. Así, abren nuevas posibilidades para combatir algunos de los cánceres más crueles que existen.
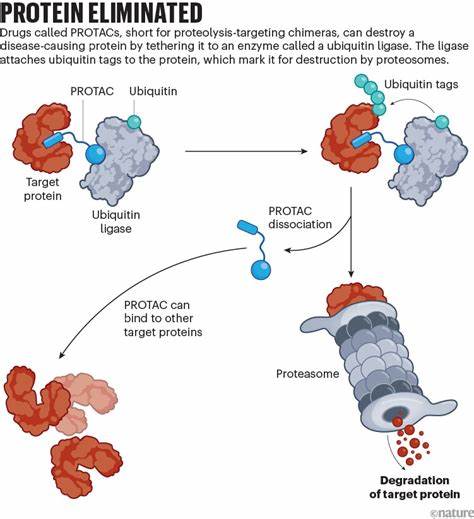
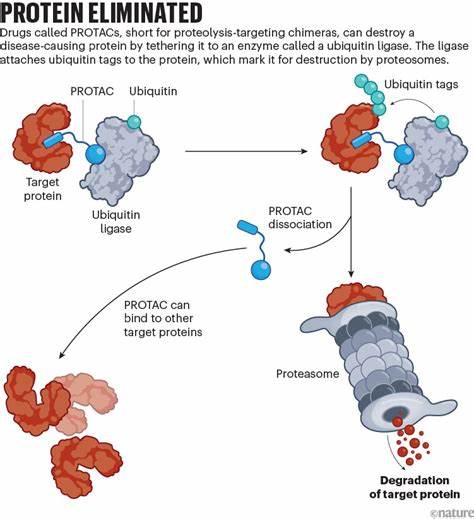
Los PROTACs funcionan de manera muy diferente a la mayoría de los fármacos tradicionales. Mientras que los medicamentos convencionales suelen bloquear la actividad de una proteína específica impidiéndole funcionar, los PROTACs utilizan el propio sistema de eliminación celular para destruir esa proteína por completo. Lo hacen mediante un mecanismo que se describe como un “beso de la muerte”: el PROTAC une la proteína dañina a una enzima llamada ubiquitina ligasa, que etiqueta a la proteína para su degradación. Este etiquetado activa el reciclaje natural de la célula, que descompone y elimina la proteína objetivo. La clave está en que los PROTACs no necesitan bloquear un sitio específico ni interferir en la función directa de la proteína, sino simplemente marcarla para que sea destruida, lo que amplía enormemente la lista de proteínas que pueden ser atacadas.
Uno de los mayores desafíos en oncología ha sido la dificultad de diseñar tratamientos efectivos contra proteínas que no tienen sitios claros para que un fármaco las bloquee, lo que las convierte en objetivos “indrugables”. Muchas proteínas implicadas en la progresión y agresividad de ciertos cánceres, como la neuroblastoma infantil, la leucemia, y algunos tumores cerebrales y de tejidos blandos, pertenecen a esta categoría. Hasta ahora, la ausencia de tratamientos específicos para estas proteínas ha limitado las opciones terapéuticas y ha aumentado la mortalidad asociada. El caso de Evan Lindberg, un niño diagnosticado con neuroblastoma a los tres años, ilustra el impacto devastador de estas enfermedades. A pesar de someterse a múltiples tratamientos convencionales como quimioterapia, radiación, inmunoterapia y cirugías, su tumor se extendió y resistió.
Su historia puso en evidencia la urgente necesidad de nuevas estrategias terapéuticas que fueran más específicas, eficaces y menos tóxicas. Investigadores como la oncóloga pediátrica Yael Mossé han dedicado décadas a buscar soluciones para estos cánceres, y han encontrado en la tecnología PROTAC una esperanza concreta para revolucionar el tratamiento de la neuroblastoma y otros tumores infantiles. El entusiasmo por los PROTACs ha crecido desde que en 2001 se demostró por primera vez su capacidad para degradar proteínas objetivo en el laboratorio. Sin embargo, inicialmente esta tecnología fue recibida con escepticismo, ya que parecía más un truco experimental que una vía viable para el desarrollo de medicamentos. Los avances tecnológicos y la mejor comprensión de la maquinaria celular permitieron superar obstáculos clave, como reducir el tamaño de estas moléculas para que pudieran penetrar en las células y seleccionar las ligasas más abundantes y eficientes para lograr una degradación eficaz.
En 2015, múltiples estudios marcaron un punto de inflexión al demostrar que los PROTACs podían eliminar casi por completo ciertas proteínas en células y modelos animales, con dosis muy bajas y efectos duraderos. Este mecanismo de acción también implica que, a diferencia de los inhibidores clásicos, los PROTACs pueden funcionar con un contacto breve con la proteína, marcándola para que la célula la elimine y luego continuar atacando otras moléculas, lo que los hace más potentes y menos propensos a resistencias. Hoy en día, hay más de treinta PROTACs en ensayos clínicos, principalmente para tratar diferentes tipos de cáncer, aunque también se exploran aplicaciones para enfermedades neurodegenerativas, inflamatorias y del dolor. Algunos de los PROTACs más avanzados están en la fase III de ensayos clínicos, enfrentándose a cánceres de mama, próstata y leucemia, ofreciendo nuevos modelos de tratamiento al degradar proteínas que ya habían sido objeto de fármacos aprobados pero que generan resistencia con el tiempo. En el campo de la oncología infantil, el equipo liderado por Mossé aspira a ir aún más lejos al apuntar proteínas que nunca han sido tratadas antes, incluyendo factores de transcripción como MYCN, una proteína que juega un papel clave en el desarrollo y agresividad de muchos tumores infantiles.
Estos factores suelen ser considerados indrugables, pero los PROTACs podrían ser la solución al eliminarlos directamente. El proyecto KOODAC (Knocking Out Oncogenic Drivers and Curing Childhood Cancers) reúne a científicos de varios países y defensores de pacientes, incluyendo a los padres de Evan Lindberg, para desarrollar estos nuevos fármacos con la ambición de hacerlos accesibles y asequibles incluso en regiones con recursos limitados. Una ventaja importante de los PROTACs radica en su capacidad para eliminar proteínas que contienen errores genéticos, como las proteínas de fusión, resultado de la combinación anormal de genes durante el desarrollo tumoral, y que actúan como potentes motores de muchos cánceres infantiles agresivos. El trabajo conjunto entre equipos multidisciplinarios y la colaboración internacional son esenciales para avanzar en esta nueva frontera de la medicina oncológica. Sin embargo, también existen retos importantes.
La complejidad biológica de los cánceres implica que erradicar una sola proteína puede no ser suficiente, ya que los tumores suelen encontrar vías alternativas para crecer y resistir. Además, la seguridad, la estabilidad y la formulación de estos medicamentos requieren más optimización para garantizar su eficacia en pacientes humanos. No obstante, la comunidad científica ve en esta tecnología un cambio de paradigma que podría transformar la manera en que abordamos el cáncer y otras enfermedades relacionadas con proteínas problemáticas. Los primeros datos de ensayos clínicos avanzados son prometedores. Por ejemplo, un PROTAC llamado vepdegestrant, diseñado para degradar el receptor de estrógeno en ciertos cánceres de mama, mostró resultados superiores frente a tratamientos estándar en pacientes con mutaciones específicas, lo que podría acelerar su aprobación.
Otros PROTACs están siendo evaluados para cánceres de próstata y leucemia, buscando superar la resistencia a los tratamientos actuales. El futuro de los PROTACs parece brillante y multifacético. Su capacidad para expandir el universo de proteínas tratables abre una nueva dimensión en el desarrollo farmacéutico, con implicaciones que van mucho más allá del cáncer. Esta tecnología podría revolucionar la medicina personalizada, permitiendo tratamientos adaptados a las particularidades genéticas y moleculares de cada paciente. En conclusión, los medicamentos degradadores de proteínas están irrumpiendo con fuerza en el panorama oncológico, ofreciendo una nueva esperanza para pacientes con cánceres hasta ahora incurables, especialmente en la infancia, donde la necesidad de terapias dirigidas y menos tóxicas es urgente.
Aunque aún quedan por superar desafíos científicos y clínicos, la evidencia acumulada y el ritmo de innovación indican que estamos ante un avance que puede cambiar profundamente la lucha contra algunos de los cánceres más crueles que afectan a la humanidad.