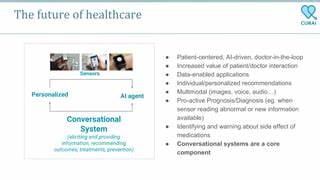
En el ámbito de la oncología, el cáncer de pulmón no microcítico representa uno de los desafíos más complejos debido a su alta incidencia y variabilidad en la respuesta al tratamiento. En este contexto, la evolución tecnológica ha permitido el desarrollo de herramientas de inteligencia artificial (IA) capaces de analizar grandes volúmenes de datos y apoyar a los médicos en la toma de decisiones. Sin embargo, a pesar de los avances en modelos de aprendizaje profundo y radiomics, persisten dificultades relacionadas con la integración de diferentes fuentes de información y la interpretabilidad clínica de los resultados. Aquí surge el concepto de un marco multimodal Doctor-in-the-Loop, una innovadora aproximación que involucra directamente al especialista en oncología dentro del proceso de entrenamiento y evaluación del modelo para lograr predicciones más precisas y explicables sobre la respuesta patológica en pacientes sometidos a terapia neoadyuvante. La multiplicidad de datos disponibles sobre un paciente con cáncer de pulmón, desde imágenes médicas hasta datos clínicos, plantea una oportunidad única para construir sistemas inteligentes que logren apreciaciones diagnósticas más completas.
Tradicionalmente, muchos modelos se han concentrado en un solo tipo de información, como las imágenes de tomografía computarizada o las características clínicas aisladas, limitando así la capacidad para captar la complejidad integral del tumor y su comportamiento. El enfoque multimodal supera esta barrera al fusionar información derivada de diversas modalidades, generando una representación enriquecida que potencia la precisión predictiva. El aspecto innovador del modelo Doctor-in-the-Loop es la incorporación directa del conocimiento y experiencia clínica dentro del bucle de aprendizaje automático. Lejos de construir sistemas autónomos, el método promueve una interacción constante entre inteligencia artificial y especialistas, permitiendo que el modelo aprenda a enfocar la atención de manera progresiva desde regiones pulmonares amplias hacia lesiones específicas identificadas como críticas por los médicos. Esta metodología no solo mejora la capacidad de predicción sino que también asegura que las decisiones automatizadas sean transparentes y explicables, facilitando la confianza y aceptación en entornos hospitalarios.
La explicabilidad en los modelos de IA es indispensable en medicina, donde la toma de decisiones impacta directamente en la vida de los pacientes. La posibilidad de visualizar qué características o regiones del tumor están influyendo en la predicción permite validar clínicamente el sistema, detectar posibles sesgos y realizar ajustes para mejorar su desempeño. En el contexto del cáncer de pulmón, donde la heterogeneidad tumoral es elevada, esta capacidad de interpretación aporta valor añadido a la evaluación personalizada del tratamiento. El entrenamiento del modelo se realiza mediante una estrategia de fusión intermedia que integra de forma eficiente las diferentes fuentes de datos, maximizando las interacciones relevantes entre modalidades sin incrementar innecesariamente la complejidad computacional. Además, el feedback clínico constante hace posible un aprendizaje supervisado enriquecido, donde los especialistas guían la atención del modelo evitando distracciones o interpretaciones erróneas.
Los resultados de este enfoque demuestran un incremento significativo en la exactitud predictiva frente a métodos unimodales o basados únicamente en características radiológicas tradicionales. Esto se traduce en una mejor identificación temprana de pacientes que responderán favorablemente a la terapia neoadyuvante, optimizando el diseño de planes terapéuticos personalizados y mejorando los pronósticos clínicos. Además, la integración multimodal permite descubrir patrones complejos que no serían detectables con análisis convencionales, aportando nuevas perspectivas a la investigación oncológica. Otro valor agregado es la facilitación de colaboración interdisciplinaria, dado que el Doctor-in-the-Loop promueve una relación de co-creación entre especialistas en oncología, radiólogos, investigadores en inteligencia artificial y bioinformáticos. Esta dinámica de trabajo conjunto no solo aumenta la calidad y robustez del modelo, sino que también impulsa la adopción tecnológica en centros clínicos, acortando la brecha entre investigación y práctica médica.