Los biofilms bacterianos representan uno de los mayores desafíos para la medicina moderna debido a su alta resistencia frente a terapias antimicrobianas convencionales. Estas comunidades microbianas complejas se adhieren a superficies biológicas o industriales formando una matriz protectora que dificulta la penetración y eficacia de los medicamentos. Este fenómeno provoca infecciones crónicas, de difícil tratamiento y con elevado riesgo de recurrencia, especialmente en pacientes hospitalizados o con enfermedades crónicas como fibrosis quística y heridas diabéticas. La innovadora combinación de antimicrobianos encapsulados en sistemas nanoscópicos activados por ultrasonido está emergiendo como una solución prometedora para superar los obstáculos que impiden el éxito terapéutico. La liberación dirigida y controlada de fármacos en el entorno del biofilm permite no solo una mayor penetración del agente antimicrobiano, sino también una perturbación física de la matriz biofilm que favorece la erradicación total de las bacterias, incluyendo las células resistentes conocidas como persister.
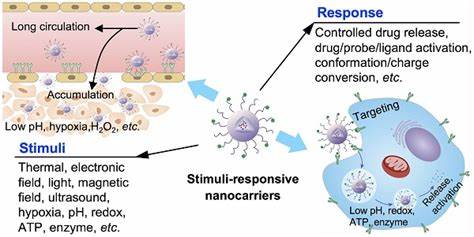
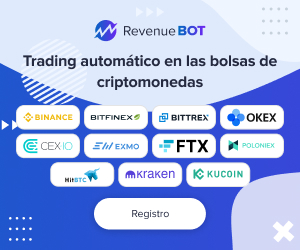
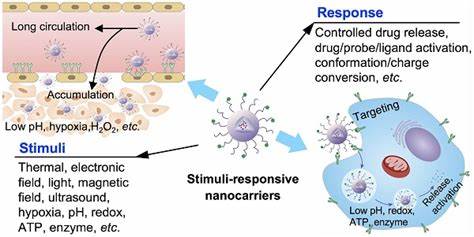
Los sistemas nanotecnológicos basados en nanodrones líquidos, recubiertos con fosfolípidos y cargados con diferentes clases de antimicrobianos, funcionan como vehículos diseñados para circular hasta la zona infectada y liberar localmente el medicamento bajo la activación específica de ultrasonido de alta frecuencia. Este enfoque combina las propiedades mecánicas del ultrasonido, capaz de generar cavitación acústica y romper la estructura del biofilm, con la farmacocinética mejorada de los antimicrobianos protegidos y transportados en formato nano. Una de las grandes ventajas de esta tecnología es su capacidad para reducir significativamente la concentración necesaria de antibióticos para alcanzar niveles bactericidas mínimos frente a agentes patógenos comunes, tanto Gram positivos como Gram negativos. Por ejemplo, investigaciones recientes demostraron reducciones de hasta 44 veces en las concentraciones de antibióticos requeridas para eliminar biofilms, en comparación con el uso de fármacos libres. Esto no solo mejora la eficacia terapéutica, sino que también puede disminuir efectos secundarios sistémicos y la presión selectiva que conduce a la resistencia antimicrobiana.
Entre los antimicrobianos estudiados están compuestos variados que incluyen antibióticos macrólidos como la azitromicina, fluoroquinolonas como la besifloxacina, péptidos antimicrobianos como la polimixina B y complejos metálicos de ruthenio con propiedades antibacterianas. Todos estos pueden ser incorporados dentro de la nanosfera con diferentes modos de acción, beneficiándose del efecto sinérgico del ultrasonido para potenciar su liberación y penetración intra-bacteriana. El proceso de activación mediante ultrasonido utiliza pulsos focalizados que inducen la vaporización controlada de los nanodrones líquidos, transformándolos temporalmente en microburbujas. Estas microburbujas oscilan y colapsan varias veces, generando fuerzas mecánicas que disgregan la matriz del biofilm y abren caminos para que los antimicrobianos accedan a las capas más profundas del biofilm. Además, esta interacción facilita que las sustancias activas se acumulen en compartimentos intracelulares esenciales, incrementando la concentración dentro de la membrana y el citoplasma bacteriano.
Este método supera una limitación crítica que enfrentan los antibióticos convencionales: su escasa penetración hasta las células bacterianas dormantes o fenómenos de resistencia intensificada dentro de la matriz biofilm. Con la liberación local de antimicrobianos, no solo se aumenta la biodisponibilidad sino que se limita la exposición sistémica, lo cual ayuda a evitar impactos negativos en microbiotas beneficiosas y reduce la probabilidad de que las bacterias desarrollen resistencia. La estabilidad y biodisponibilidad de estas plataformas basadas en nanodrones han sido ampliamente caracterizadas, evidenciando una adecuada resistencia a la degradación y una vida útil que permite aplicaciones clínicas viables. Además, la utilización de componentes aprobados o relacionados con agentes de contraste clínicos facilita su incorporación en procesos terapéuticos ya existentes, acelerando su traducción a entornos médicos. Por otro lado, la tecnología de ultrasonido aplicada posee una excelente curva de seguridad y versatilidad, lo que abre la puerta a tratamientos no invasivos con capacidad de ser guiados en tiempo real mediante imagenología, mejorando la precisión y minimizando efectos en tejidos sanos circundantes.
Los resultados en modelos clínicos y simulados de infecciones crónicas como infecciones en articulaciones protésicas, infecciones urinarias, heridas crónicas y fibrosis quística confirman la eficacia generalizada de estos sistemas, eliminando tanto células activas como persister y limitando la dispersión no controlada del biofilm, que podría ocasionar sepsis o recolonización en otros sitios. El impacto de esta tecnología en la medicina no se limita a la terapia antibacteriana. La plataforma de liberación basada en ultrasonido permite, en el futuro, integrar agentes antibiofilm adicionales, tales como enzimas que degradan la matriz polimérica o gases bioactivos con propiedades terapéuticas específicas, ampliando el abanico terapéutico y adaptándose a diversas patologías y tipos de biofilm. El avance y desarrollo de sistemas antimicrobianos activados por ultrasonido con nanodrones encapsulados marca un antes y un después en el abordaje de infecciones complejas. Al superar de manera eficiente las barreras biológicas y mejorar la entrega intracelular de fármacos, esta tecnología ofrece una estrategia robusta para enfrentar la alarmante problemática de las infecciones persistentes y la resistencia antimicrobiana global.
Para el futuro, es esencial continuar con investigaciones centradas en la optimización del diseño de nanocarriers, la dosificación ultrasonográfica y el estudio minucioso de su interacción con diferentes tipos bacterianos y tejidos humanos. Asimismo, la evaluación de su seguridad e impacto inmunológico será clave para asegurar su implementación clínica a gran escala. En conclusión, la sinergia entre nanotecnología y ultrasonido representa una innovadora frontera para la medicina antibiótica, destinada a transformar el manejo de infecciones biofilm, reducir los costos asociados a tratamientos prolongados y mejorar la calidad de vida de millones de pacientes en todo el mundo.